8例小儿体外膜式氧合支持治疗回顾分析
傅惟定,张蔚,王伟,姜磊,沈佳,唐嘉忠,朱德明
(上海交通大学医学院附属上海儿童医学中心心胸外科 上海200127)
摘要:目的 总结小儿先心术后严重心力衰竭和暴发型心肌炎应用体外膜肺氧合(ECMO)支持治疗的经验。方法 8例ECMO中心内直视术后不能脱离CPB7例,暴发型心肌炎1例。全组均使用离心泵。全部静脉一动脉模式,采用中心插管,右房一升主动脉7例,周围大血管插管,股静脉一股动脉模式1例,辅助时间65~498h,辅助流量80~120ml/(min.kg)。结果死亡5例,出院3例,存活率38%,并发症包括,出血5例,血栓形成2例,溶血1例,DIC1例,肝衰竭1例,营养不良2例,机械故障2例。结论 先心术后无残余解剖畸形,而出现严重心衰病例,宜及时施行ECMO支持治疗,及时补充新鲜血小板,血浆等血制品,加用超滤,减少机体和机械并发症,婴儿和新生儿优选ECMO。
关键词:小儿体外循环,体外膜肺氧合
Retrospective Analysis of 8 childs Managed by Extracorporeal Membrane Oxygenation in Shanghai children Medical Center.
Fu wei-ding ,Zhang wei ,Wang Wei, Jiang Lei , Shen Jia, Tang Ja -zhong
Corresponding author: Zhu De-ming ,E-mail:
(Department of Thoracic and Cardiovascular Surgery ,Shanghai children's Medical Center , school of Medicine, Shanghai Jiao Tong University, Shanghai , 200127.China)
ABSTRACT: Objectives: Sum up the exeperience of congenital heart surgery with sever heart failure postoperatively use extracorporeal membrane oxygenation (ECMO) assistant thearpy.
Methods: seven of 8 patients failure to wean from bypass and one of 8 patients with fulminant myocarditis put on ECMO Centrifugal pump . Import membrane oxygenator , Central cannulae, veno-arterial mode ECMO ,right atrirm-acending aortic 7 cases preipheral cannulae veno-femoral artery 1 case Assistant period ranged from 65~498 hrs , flow rate was maintained at 80 to 120 ml /(min.kg ) Items in comparison included blood perssure , lactic concentation of artery was significantly higher than that of post-ECMO (P<0.05) . MAP pre-ECMO in patients was significantly lower than that of post ECMO (P<0.05).
Results: 5 patients were died with the mortality 62.5%, Discharge 3 cases . Survival 38%. Bleeding 5 cases. Thrombosis 2 Cases , Hemolysis 1 case. DIC 1 case. Liver failure 1 Case . Malnutrition 2 cases. Oxygenator plasma leakage 2 cases .
Conclusions: postoperative no residule and anatomy deformity ECMO could be used established as early as possible in severe heart failure post cardiotomy. Infusion fresh blood platelet. Frozen plasma. Packed RBC and blood prodrcts. Continous arterio-venous hemofiltration . Decrease body and mechanical complications, Neonatal and infant are rather ECMO than VAD ( ventricular assist device) .
Key words: Cardiopulmonary bypass in children-Extracorporeal membrane oxygenation.Corresponding author: Zhu de ming
心脏术后部分病例因心肺功能衰竭需要ECMO支持治疗相关报道渐多,国外报道约占先心术后3~5%[1.2],上海儿童医学中心自2007年7月~2009年9月对术后严重心衰和暴发型心肌炎开展了ECMO支持治疗,报道如下:
1、资料和方法
1.1一般资料 共8例,男4例,女4例,年龄18天~3岁3月。其中年龄<1岁7例,体重3.4~12㎏,资料见表1。
1.2 ECMO建立和管理
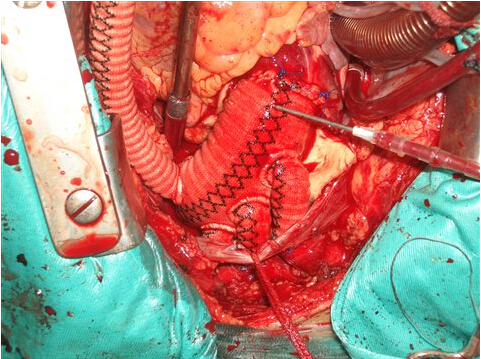
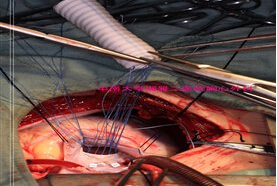
1.2.1方法 均行静脉—动脉(V-A)模式,经原手术切口右心房一升主动脉插管7例,股静脉一股动脉插管1例。勃脉力—A预充排气,体重<10㎏加入少浆红细胞150ml,氯化钙1mmol/L,右房插管用金属丝加强型直头静脉插管,经左心耳、右上肺静脉插管置左心减压。股静脉动脉转流者,加装再灌注导管插入远端股动脉。
装备 离心泵为Bio—pump plus、Delphin和Jostra,膜肺为Medtronic,Minimax plus Carmeda肝素涂层和Jostra PES肝素涂层,Carmeda CB2503R1套包,sarns水箱,自动凝血时间监测仪。
1.2.3管理 流量40~200ml/㎏.min,使静脉血氧饱合度维持>65%,膜肺出口血氧分压在150mmHg左右,转速2000转/分,维持血小板100,000/㎜3,每天补充新鲜血浆,监测游离血色素,肝素持续静脉微泵10-30µg/(kg.h)维持,所有患者均延迟关胸。血细胞比容30%~35%,活化凝血时间(activated clotting time,ACT150~180秒),在V-A回路中建立旁路,加装血液浓缩器,使用时用夹夹调节匀速进出量,如血钾和乳酸增高,在不影响血压的前提下,稍增加超滤量,同时调高辅助流量,维持体温35-37℃,ECMO支持期间减量或停用心血管活性药物。
撤机:血液动力学稳定,逐步减小辅助流量,同时增加血管活性药物的用量,先钳夹左房引流,遂递减流量在10ml/min,多巴胺<10µg/(kg.min)心脏超声LVEF≥40%,尝试动脉夹管,再观察30min,血液动力学稳定则撤离ECMO。
1.3统计学处理 应用Spss13.0统计软件对数据进行t检验,以均数±标准差(x±s)表示。P< 0.05为有统计学意义。
2、结果 死亡5例,康复出院3例,存活率37%,出血(5例,62.5%),血栓形成(2例,25%),DIC(1例,12.5%),溶血(1例,12.5%),肝衰竭(1例,12.5%),营养不良(2例,25%),膜肺血浆渗漏氧合器置换(2例,25%),机械故障(2例,25%)辅助时间65~498h。ECMO建立后的平均动脉血压60.2±7.8mmHg较建立前平均动脉血压48.1±5.2mmHg明显上升,具显著意义(P< 0.05),乳酸水平由5.1±0.8至3.6±0.5mmol/L下降,具显著意义(P< 0.05)。图1。
- 讨论
3.1指征 ECMO指征为低心排4例,其中不能脱离CPB3例,Nikaidoh术后次日按装1例,脱机后待续低氧血症1例,肺出血1例,体外意外1例,严重心律失常1例,为暴发型心肌炎,病情凶险选择股动静脉模式,资料见表1。先心与获得性心脏病不同,不能脱离CPB者,多有残余梗阻,残余漏或血液动力学上的问题,而后者多为换瓣或搭桥手术,仅为心功能差,不伴解剖结构异常,因此,先心必需经食道超声证实无血液动力学异常,心肺可恢复的前提下,且病人情况不能已处接近或不可逆状态。婴儿和新生儿应选ECMO而不是VAD,王伟[3]研究报道16例小儿ECMO和VAD两组出院率比较以ECMO组为高,因小儿心衰往往合并左右心室并伴肺功能不全,除外经济问题的考虑,首选ECMO,以取代肺脏气体交换功能,减少呼吸器使用中的高浓度氧气和气道压的肺损伤,慎选病例,如有适应证早用和积极的照顾患者可明显改善预后。本组COA/VSD、冠状动脉分支损伤,TGA行Nikaidoh术均无血液动力学的残余阶差或漏,仅为心功能低下。肺栓塞病例虽经一氧化氮(NO)吸入和肺泡表面活性物质治疗无法改善氧合建立ECMO,但取栓后建立ECMO无法逆转已间歇使用呼吸机13天导致的肺损伤,肺顺应性差,氧合功能低下,PaO2<40mmHg,这类机械呼吸长达7天的慢性肺损伤应为禁忌症,肺组织纤维化已呈不可逆变化,另就Gleen 术后血液动力学而言,ECMO仅氧合下半身的血,先心腔肺吻合和Fontan术等ECMO指征值得商榷。另1例TGA新生儿因主动脉插管头端顶主动脉壁引起复跳后的肺出血,虽创伤时间不长,建立ECMO后终不治,可见婴儿肺出血与成人不同,十分风险,可逆程度差。暴发型心肌炎ECMO为绝对指征,支持时间长达3周,成功撤机后未获成功,其中重度营养不良为重要原因。
3.2出凝血 人工设备经肝素涂层处理减少了肝素的应用和炎性反应的程度,降低白血球活化及血清炎性介质,但出血仍是ECMO治疗中最常见的并发症,ELSO报告ECMO出血的发生率为29%[4],本组8例病例中,有5例发生出血,占62.5%,肝素抗凝,大量血制品输注,无凝加重凝血机制紊乱。我们采用的原则为ECMO当天,主要监测出血,48小时后以防止血栓形成为主要目标,根据出血部位及出血量处理不同,插管及手术切口部位小面积渗血,采取局部压迫,调整肝素用量或间断停止肝素输注的方法,降低ACT,促进凝血,维持血小板数,监测PT、PTT,必要时输注纤维蛋白元、FDP等,维护血液动力学稳定,防止心包填塞以及局部用明胶海绵止血,胃肠道出血用冷生理盐水洗胃和用抗酸剂。腹腔出血手术探查3次1例,发现出血点在右髂窝股动脉穿刺处。管道内血栓形成1例。蛛网膜下腔出血和超声疑左室内血栓形成1例,并有严重溶血和血色素尿,游离血色素>100mg/dl,北京阜外医院袁媛回顾分析了107例体外膜肺氧合支持治疗中有左室内血栓形成1例,认为原因可能为体外引流量大,导致左房内血流减少,速度减慢所致[5],减低转速,碱化尿液,补充新鲜血小板,血浆和新鲜血是针对出血的主要措施,新鲜血浆含有AT-Ш,可弥补因肝肾功能损伤、DIC导致的获得性AT-Ш缺乏,和新生儿、小婴儿AT-Ш浓度不足,纠正肝素抗凝异常,ECMO支持3周的后期因未稍微血管栓塞,指趾端皮肤出现发黑坏死,出院二周随访发现坏死皮肤渐脱落后恢复正常
3.3操作失当和机械故障 早期建立ECMO即出现气体,不得不重新排气,主要原因是血容量不足和静脉引流差,X线和超声发现静脉插管头端在二尖瓣内1例,静脉引流管扭曲1例,通过注意容量补充,降低泵转速和调整静脉插管位置近期已无再次发生。
离心泵在前负荷增加或后负荷减低时,泵流量升高。转速不变,血流量随患者全身血管阻力变化自动调节,争取低转速高流量,对组织脏器包括心肌功能的恢复至关重要,在氧代谢和血流动力学稳定的前提下,应争取最大辅助流量和注重流量平衡,增加流量时,静脉端负压不宜>-40mmHg。流量低于转速,可能输出端有扭曲梗阻或外周阻力大,应注意调整管道或用药物降低外周阻力。离心泵头内血栓形成1例,膜后压力达330mmHg,泵头顶端可见白色血栓,出现机械转运异常声音和溶血,血浆游离血红素高达7.6,有血色素尿,灌注管有抖动与抗凝不足、血流缓慢有关。
据ECLO统计报道氧合器血浆渗漏发生率7.1~16.7%[4],使用Medtronic Minimax膜肺的患者出现溶血,膜肺血浆渗漏和更换膜肺的发生率显著高于Jostra Quadrox膜肺,据研究Medtronic膜肺使用微孔中空纤维,因而血浆渗漏的几率较高[5],本组Medtronic氧合器渗漏2例,使用3天左右出现膜肺底座接水管处有血浆渗漏,血液进入气室引起氧合能力下降,均更换氧合器,其中1例先后换Medtronic 3次,另1例使用Medtronic 3天膜肺后换用Jostra硅胶微孔氧合器(Plasma resistant fiber PRF)使用时间达3周无血浆渗漏且氧合良好。有研究结果表明,Jostra Quadrox D膜肺使用新型膜肺材料聚甲基戊烯致密中空纤维,具有疏水性,增加血液相和气相的分离度,从而避免血浆渗漏并延长了氧合器的使用时限[6、7],血浆渗漏与氧合器类型、跨膜压差、辅助流量、血液破坏程度有关,其中血液破坏产生的游离血红蛋白及其代谢产物对氧合器有潜在威胁[8]。
3.4 超滤 复杂先心手术中深低温停循环,长时间转流和纠治不理想等因素往往会导致术后低心排,肾脏持续性低灌注、缺血缺氧,引起少尿型肾衰,常规腹膜透析常因腹腔出血不得不减少透析次数或缓透,本组在ECMO管路中按装血液超滤6例,通过钳夹动静脉控制滤出量,能有效减少细胞外液和降低血钾,控制容量负荷,改善氧合和提高心输出量,每小时滤出20~100ml不等,滤出过程注意观察中心静脉压,血压变化,并监测血清尿素氮、肌酐和K+相应参数,注意在血滤过度时,可影响ECMO整体血液,本组未发现有与超滤相关并发症的发生。
表1 ECMO支持治疗患者的临床资料
|
编号 诊断 手术名称 指征 并发症 结果 |
|
1 TGA/IVS/ASD ASO 肺出血 出血、DIC 死亡 2 TOF 根治 灌注心肌保护液 肝衰竭 死亡 冠状动脉进气 3 TOF二期 根治 冠状动脉分枝切断 机械故障 出院 4 TGA.VSD Nikaidoh 心衰 微循环栓塞 出院 5 VSD.COA 根治 心衰 出院 6 TGA.双侧腔肺 取栓 低O2 血栓 死亡 吻合术后肺栓塞 7 暴发型心肌炎 — 严重心律紊乱心衰 低O2出血、感染 死亡 营养不良 8 PA/VSD二期 根治 心衰 营养不良、出血 死亡 神经系统 |
注:TGA:大血管错位;IVS:室隔完整;TOF:法乐氏四联症;ASD:房间隔缺损;VSD,室间隔缺损;COA:主动脉缩窄,PA:肺动脉瓣闭锁;Nikaidoh:主动脉换位手术;ASD:大动脉调转手术;DIC:弥漫性血管内凝血。
100—
80—
60— P<0.05
40—
20—
0—
ECMO 前 ECMO后
图2 ECMO建立前后血压变化
10—
8—
6—
P<0.05
4—
2—
0—
ECMO 前 ECMO后
图1 ECMO建立前后血乳酸水平变化
参与文献
[1] Brown KL,Goldman AP, Neonatal extra-corporeal life support: indications and limitations[J].Early Hum Dev,2008,84(3):143-148.
[2] Ghez O, Feier H,Ughetto F,et al. Postoperative extracorporeal life Support in pediatric cardiac surgery : recent results [J] ASAIO.J,2005,51(5):513-516.
[3] 王伟等,儿童心脏辅助设备的使用和选择,第四届中国体外循环会议,成都2009。
[4] Conrad SA,RycusPT, Dalton HJ,et al Extracorporeal Life Support Registry Report 2004 [J] .ASAIO J ,2005, 51(1):4-10.
[5]袁媛等,北京阜外医院107例体外膜肺氧合支持治疗回顾分析,2009成都会议,第四届中国休外循环会议。
[6] Meyns B, Vercaemst L, Vandezande E ,et al. Plasma leakage of oxygenators in ECMO depends on the type of oxgenator and on. patient variables [J] . Int J Artif Organs .2005, 28(1):30-34.
[7] Horton S , Thuys C, Bennet M, etal.Experience with the Jostra Rotaflow and Q uadrox D oxygenators for ECMO [J].Perfusion,2004,
19(1):17-23.
[8] Levi D, Marelli D, Plunkett M, et al .Use of assist devices and ECMO to bridge pediatric patients with cardiomyopathy to transplantation[J]. J Heart Lung transplant, 2002, 21 (2):760-770.
君健网(www.junjian99.com)专稿,转载方请明确注明出处及链接,或完整保留此版权信息。
肺动脉灌注HTK液在法乐氏四联症矫... 上一篇 | 下一篇 钙预处理对未成熟心肌保护作用的研...
- 经胸右室穿刺封堵婴儿室间隔缺损25例报告2014-12-15
- 风湿性心脏病瓣膜置换术后焦虑与抑郁状况分析2014-12-10
- 高海拔地区59例双瓣膜置换术的临床分析2014-12-10
- 肺动脉夹层动脉瘤综述2014-12-15
- 马凡综合征主动脉根部瘤的改良Bentall术治疗2014-12-15
- 深低温停循环后梯度灌注复温脑保护的实验研究2014-12-15
- 组织工程血管基质的制备及保存2014-12-15
- 胸腔镜下体外循环心脏手术10例报道2014-12-15
- 原位心脏移植患者术后远期随访与分析2014-12-15
- 全球首个在“移植子宫”内孕育的婴儿降生2014-12-10
-
医生姓名:刘伏友
所在科室:肾内科
工作医院:中南大学湘雅二医院
专业职称:主任医师
擅长疾病: 腹膜透析、各类肾病、慢性肾功能衰竭、尿毒症、血液...